آلومینیوم عنصری شیمیای در گروه بورون با عدد اتمی ۱۳ و نماد Al است. این عنصر یک فلز نرم، سفیدوچکشپذیر با چگالی پایین است که سومین عنصر فراوان و فراوانترین فلز در پوسته کره زمین است. آلومینیوم خالص به دلیل واکنشپذیری بسیار بالای خود بسیار به ندرت به طور طبیعی یافت میشود به صورت ناخالص در سنگهای معدنی مختلفی وجود دارد. بیشتر آلومینیوم دنیا از سنگ بوکسیت به دست میآید.
 نامگذاری آلیاژهای آلومینیوم
نامگذاری آلیاژهای آلومینیوم
آلیاژهای آلومینیوم به دلیل داشتن خواص منحصر به فردی مانند نسبت استحکام به وزن بالا، جوش پذیری خوب، شکل پذیری عالی و مقاومت به خوردگی نسبتاً خوب، به گونه گسترده در انواع سازهها، صنایع هوایی و دریایی، خطوط انتقال برق، حمل و نقل و… استفاده میشوند. با اضافه کردن عناصری مانند مس، روی و سیلیسیوم به آلومینیوم میتوان به خواص مکانیکی بهینه رسید. در برخی آلیاژهای آلومینیوم لازم است عملیات ترمومکانیکی انجام شود. در این عملیات که بیشتر ویژه آلیاژهای سری ۲۰۰۰ ،۷۰۰۰ و ۶۰۰۰ است، ذرات در مرزدانهها رسوب کرده و در نتیجه نواحی اطراف مرزدانهها از عنصر آلیاژی تهی میشوند و این خود میتواند شروعی برای خوردگی موضعی بویژه خوردگی حفرهای و بین دانهای باشد؛ بنابراین، آلیاژهای آلومینیوم با استحکام بالا مانند ۲۰۲۴ ،۷۰۷۵ و ۶۰۶۱ که در صنایع گوناگون کاربرد فراوانی دارند، حساسیت زیادی به خوردگیهای موضعی بویژه حفرهای و بیندانهای دارند. این نوع خوردگیها میتوانند شروعی برای انواع خوردگی مثل پوستهای شدن (Exfoliation)، خوردگی تنشی SCC و ترکهای خستگی در آلیاژهای آلومینیوم باشند. فرایندهایی مانند عملیات حرارتی محلول جامد، کوئنچ و رسوبسختی، اثر قابل ملاحظهای بر ترکیب شیمیایی موضعی آلیاژهای با استحکام بالا و قابل عملیات دارد.
به طور کلی به علت وجود میزان کمی آب در ساختار آلومینیوم هر نوع عملیاتی که باعث از بین رفتن یکنواختی در میکروساختار آلیاژ شود مقاومت به خوردگی را کاهش میدهد بررسی خوردگی موضعی آلیاژهای آلومینیوم مورد نظر در محیطهای هالیدی از اهمیت بالایی برخوردار است. محیطهای هالیدی شامل یونهای کلرید و یا برومید میتوانند لایه رویین روی سطح آلومینیوم را بشکنند و سبب ایجاد خسارت روی سطح شوند. از سوی دیگر، در این آلیاژها استحکام با انجام عملیات حرارتی و با رسوب ترکیبات شامل مس، روِی و منیزیوم افزایش مییابد. انحلال این رسوبات در دماهای بالا (حدود ۴۸۰ درجه سانتی گراد) محلول فوق اشباع از این عناصر را بوجود میآورد که تحت عملیات حرارتی، ترکیبات ریز شامل این عناصر رسوب میکنند. رشد همین ترکیبات، سبب ایجاد ساختاری ناهمگون شده که افزون بر کاهش استحکام، در رشد لایه پسیو تشکیل شده چه در هوا و چه در محیطهای آبی، اخلال به وجود میآورند.
از این رو، محل شروع حفرهدارشدن را میتوان به نقاط ضعیف در لایه پسیو مرتبط دانست. برخلاف فلزات دیگر که خوردگی باعث کاهش کلی ضخامت میشود در آلومینیوم خوردگی تمایل دارد به صورت موضعی در سراسر سطح، حفرات زیادی تولید کند و در کل بخش وسیعی از سطح دست نخورده باقی میماند. تا کنون پژوهشهای زیادی در رابطه با خوردگی موضعی آلیاژهای آلومینیوم در محلولهای کلریدی انجام گرفته است. برای مثال، در سال ۲۰۰۴ سینیاوسکی و کالینین به بررسی خوردگی آلیاژهای آلومینیوم در آب دریا پرداختهاند، ولی در مجموع کمتر به موضوع خوردگی اتمسفری پرداخته شده است. بتازگی کوزنیکا در سال ۲۰۰۹ در مورد آلیاژ ۲۰۱۷، لی و همکارانش روی آلیاژ ۲۰۱۲ و نایت و همکارانش در سال ۲۰۱۱ در مورد آلیاژهای ۲۰۲۴ و ۷۰۵۰مقالاتی در این زمینه به چاپ رساندهاند.
خوردگی اتمسفری نوع خاصی از خوردگی بوده که به علت تشکیل یک لایه الکترولیت روی سطح که بیشتر فیلم نازکی از رطوبت است، بوجود میآید. ضخامت این لایه از ۱۰۰ میکرومتر تجاوز نمیکند و میتوان فرض کرد این لایه همیشه اشباع از اکسیژن است. وقتی فلز در آب یا محلول نمکی مانند کلرید سدیم غوطه ور است بدلیل کاهش نفوذ اکسیژن در نواحی کاتدی نرخ خوردگی کاهش مییابد، ولی در خوردگی اتمسفری به دلیل اینکه گاهی لایه الکترولیت روی سطح خشک میشود یک شرایط تناوب خشک و تر بوجود میآید که باعث تشدید خوردگی نیز میشود. یون کلر نقش اصلی در خوردگی را ایفا میکند. مقدار خورندگی محیط به شدت تابع غلظت یون کلر در اتمسفر است. یون کلر باعث تخریب و سوراخ شدن لایه اکسیدی محافظ میشود.
 تاریخچه کشف آلومینیوم
تاریخچه کشف آلومینیوم
آلومینیوم موجود در پوسته زمین تماماً بصورت ترکیبی است و ۷٫۵ درصد کل پوسته زمین را تشکیل می دهد که پس از اکسیژن (۴۹٫۲ درصد) و سیلیسیم (۲۵٫۸ درصد) سومین عنصر فراوان از نظر کمیت بوده است. این در حالیست که آهن پر مصرف و قدیمی صرفا ۴٫۳ درصد پوسته زمین را تشکیل می دهد.
باوجود آنکه امروزه آلومینیوم پس از فولاد پر مصرف ترین فلز جهان محسوب می شود ،اما پیشینه وسابقه تولید این فلز حتی به دو قرن هم نمی رسد ودر مقایسه با فولاد و مس که از فلزات دیر آشنای صنعت هستند فلزی جوان محسوب می شود که توانسته است با عمری کوتاه ،جایگاه مصرفی وارزش بالایی را در صنایع مختلف به خود اختصاص دهد. دلیل عمرکوتاه وعدم استفاده از این فلز در سالهای پیشین، نوع سنگ معدن و نحوه استخراج آلومینیوم از آن می باشد.
مشکل وهزینه بر بودن استخراج آلومینیوم از سنگ معدن اکسیدی آن (روش الکترولیز)باعث تاخیر حضور این فلز در توسعه صنعتی تا سالهای پس از آغاز قرن نوزدهم شد.
افتخار تولید اولین قطعات آلومینیوم خالص فلزی به شیمیست دانمارکی بنام اورستد(H.C.Oersted) تعلق دارد. هر چند که او نتوانست برای بار دوم آزمایش خود را با موفقیت تکرار کند اما همکار جوان او وهلر(F.Wohler) در سال ۱۸۲۷، از واکنش AlCl3 با پتاسیم فلزی، توانست بقدر کافی آلومینیوم خالص تولید نماید.(AlCl3 +۳K = Al + 3KCl)

قیمت یک کیلوگرم از این آلومینیوم تولیدی در حدود ۱۲۰۰ دلار بود، به گونه ای که گفته می شود در قصر ناپلئون سوم از ظروف آلومینیومی به جای ظروف طلا جهت پذیرایی میهمانان ویژه استفاده می شد
تهیه آلومینیوم در مقیاس تجاری برای اولین بار در سال ۱۸۵۵ توسط سن کلردویل(H.S.C.Deville) انجام شد. او توانست قیمت یک کیلو گرم آلومینیوم را به حدود ۳۷ دلار برساند. با این حال، آلومینیوم نتوانست درآن زمان جایگاه اصلی خود را بیابد.
افتخار تولید اولین قطعات آلومینیوم خالص فلزی به شیمیست دانمارکی بنام اورستد(H.C.Oersted) تعلق دارد. هر چند که او نتوانست برای بار دوم آزمایش خود را با موفقیت تکرار کند اما همکار جوان او وهلر(F.Wohler) در سال ۱۸۲۷، از واکنش AlCl3 با پتاسیم فلزی، توانست بقدر کافی آلومینیوم خالص تولید نماید.(AlCl3 +۳K = Al + 3KCl)

بالاخره در سال ۱۸۸۶ دانشمند آمریکائی C.M.Hall و دانشمند فرانسوی P.L.Heroult بطور همزمان و جداگانه موفق شدند که با حل کردن آلومینا در کریولیت مذاب و عبور دادن جریان برق، از محلول الکترولیتی بدست آمده فلز آلومینیوم را جدا نمایند. این دو دانشمند هر دو متولد ۱۸۶۳ (اولی در تاریخ ۶ دسامبر و دومی در تاریخ ۱۰ آوریل) C.M.Hall در امریکا و P.L.Heroult در فرانسه بودند .
هردو جداگانه در یک زمان (۱۸۸۶) اساس تولید آلومینیوم بطریق الکترولیز مذاب اکسید آلومینیوم حل شده در کریولیت را آنچنانکه امروزه متداول است بنام خود ثبت و راه نوینی را در جهت تولید یکی از مهمترین فلزات گشودند.
جالبترین مطلب در مورد این دو دانشمند آن بود که گر چه هر یک مستقل و بافاصله هزاران کیلو متر دور از هم در کشور خود به تحقیق مشغول بودند ولی به فاصله دو ماه تقاضای ثبت کار خود را از کشورهای خود نمودند. تاریخ تقاضای Heroult در ۲۳ آوریل ۱۸۸۶ وHall در ۹ ژوئیه همان سال بود . این کشف به اسم، هال و هرولت ثبت گردید .موضوع دیگر آنکه تاریخ فوت دو دانشمند، که هر دو در سال ۱۹۱۴، هال در تاریخ ۲۷ دسامبر و هرولت در تاریخ ۹ مه اتفاق افتاد نیز طول عمری مساوی را برای آنها بر جای گذاشت.
متعاقب این اکتشاف در سال ۱۸۸۸، بایر(K.G.Bayer) آلمانی توانست با حل کردن بوکسیت ناخالص در سود سوزآور و بدست آوردن آلومینات سدیم و حل کردن آن در آب و در نتیجه ته نشین شدن هیدرات آلومینیوم که پس از تبخیر آب هیدرات،آلومینای خالص(AL2O3)و سفید رنگی بدست میدهد، تحولی بزرگ در تهیه آلومینا بوجود آورد در نتیجه پروسس Hall-Heroult بهمراه پروسس Bayer پایه های صنعت تولید آلومینیوم را تشکیل دادندکه پس از گذشت حدود ۱۳۰ سال هنوز هم اساس تولید آلومینیوم در دنیا به همان روال ادامه دارد البته در طی این زمان تکنولوژی تولید، پیشرفتهای چشمگیری داشته است.
هال- هرولت و بایر مسئول تولید عملی آلومینیوم تجارتی محسوب می گردند. در طول مدت فقط، قیمت یک کیلو آلومینیم خالص تولیدی از ۱۲۰۰ دلار به حدود ۱٫۸ دلار رسید.
فرآیند آلکار
اصول تهیه و روش تولید از ابتدا تا به امروز فرق چندانی نکرده و در طول مدت با پیشرفت تکنولوژی بتدریج ظرفیت واحدها و راندمان تولید بالا رفته و نیز مصرف انرژی کاهش یافته است و بطور خلاصه تکنولوژی تهیه این فلز به لحاظ کمی و کیفی پیشرفت یافته است بعنوان مثال دیگهای اولیه با ابعاد کوچک با ۸ کیلو آمپر و ۳۸ کیلو وات ساعت مصرف انرژی الکتریکی برای هر کیلو گرم آلومینیوم کار می کردند ؛ در حالیکه آخرین تکنولوژی دیگهای جدید با ابعاد بزرگ و با ۶۰۰ کیلو آمپر شدت جریان و مصرف ۱۲ کیلو وات ساعت به ازای هر کیلوگرم آلومینیوم کار می کنند
عدم استفاده از فلورایدها و کربن خالص نکات جالب در گزینههای جدید هستند. از طرف دیگر پروسه هال- هر ولت مقدار متنابهی گاز تولید میکند در حالیکه پروسههای فوق تولید گاز CO مینماید و این به این معنی است که مصرف کربن به ازاء هر کیلوگرم آلومینیوم تولیدی در گزینههای جدید بیشتر از روش هال-هرولت می باشد.
مصرف برق گزینه جدید هم عامل مهمی برای ارزیابی است. پروسه هال – هرولت از نظر راندمان انرژی زیاد مناسب نیست زیرا در بهترین حالت راندمان انرژی این پروسه ۴۵ درصد است که دلیل آن از بین رفتن انرژی حرارتی دیگ و افت ولتاژ در مدار خارجی دیگ (باسبار، آند، کاتد) می باشد. یکی از مزایای دستیابی به دیگMultipolar جهت الکترولیز آلومینیوم تریکلراید، کاهش افت ولتاژ در مدار خارجی دیگ و در نتیجه صرفهجوئی انرژی است.
بوجودآوردن آندهای خنثی غیرمصرف شونده در پروسه هال-هرولت، انقلابی بزرگ در صنعت آلومینیوم است. این آند باید هادی خوبی برای برق و غیرمحلول در الکترولیت باشد. با توجه به اینکه احتمال تجاری شدن آندهای غیرمصرفشونده طی ده سال آینده وجود دارد
استفاده از آندهای خنثی نه تنها مانع از تولید گازهای گلخانه ای می شود، بلکه با استفاده از این آندها هر واحد تولیدی آلومینیوم به تنهایی به یک منبع تولیدکننده عظیم از اکسیژن بدل خواهد شد. از طرف دیگر، عدم نیاز به جایگزینی و عمر بالای این آندها در قیاس با آندهای کربنی، می تواند در کاهش هزینه های تولید کمک شایانی کند. امروزه تهیه آلومینیوم اولیه از فرآیند Hall-Hercult برای احیای آلومینا و تولید آلومینیوم بهره می برد. در این فرآیند آلومینا در الکترولیتی از مذاب کرولیت حل شده و با اعمال جریان برق مستقیمی آلومینیوم احیا می شود. به دلیل مقاومت بالای الکترولیت، اعمال جریان برای احیای آلومینیوم با گرمایش زیادی همراه است که علاوه بر مذاب نگه داشتن کرولیت، آلومینیوم احیاشده به صورت مذاب خارج می شود. عمدتاً به دلیل دمای بالای فرآیند، آندهایی نیاز است تا بتواند علاوه بر تحمل دمای بالا، رسانایی بالایی نیز در آن دما داشته باشد. از این رو عموماً از آندهای کرینی برای این منظور استفاده می شود. گرچه استفاده از آندهای کرینی مزیت های گفته شده بالا را دارد (رسانایی بالا در دمای بالا)، ولی کرین موجود در آند با اکسیژن رهاشده در هنگام احیا شدن آلومینا واکنش انجام داده و گازهای دی اکسیدکربن یا مونواکسیدکربن تشکیل می دهد. همین امر سبب می شود که به ازای هر ۲۶ تا ۳۰ روز، نیاز به جایگزینی آندهای کربنی جدید باشد. به طور کلی به ازای تولید هر تن آلومینیوم اولیه، حدود ۰٫۴-۰٫۵ تن کرین مصرف می شود، تولید گازهای گلخانهای همچون دی اکسیدکربن از ملزومات فعالیت صنعتی خواهد شد. از این منظر، استفاده از تکنولوژی های نوینی که سبب کاهش تولید گازهای گلخانه ای شود در اولویت تولیدکنندگان خواهد بود. در سالهای اخیر شرکت روسال، به عنوان یکی از شرکت های پیشرو در صنعت آلومینیوم در حال طراحی و توسعه آندهای خنثی بود که تنها امکان انجام نیم واکنش های اکسیداسیون را روی سطح الکترود فراهم می آورد و خود، وارد واکنش نمی شود. امیدوار است به زودی تکنولوژی تولید آندهای خنثی را روانه بازار نماید.
استفاده از این نوع آندها نه تنها مانع از تشکیل گاز گلخانه ای دی اکسیدکربن شده، بلکه سبب تولید گاز اکسیژن نیز می شود. به این ترتیب به ازای تولید هر تن آلومینیوم حدود ۰٫۹ تن اکسیژن خالص وارد اتمسفر می شود. به عبارتی هر سلول احیا در این فرآیند همانند یک جنگل انیوه ۷۰ هکتاری عمل خواهد کرد. استفاده از آندهای خنثی، علاوه بر مزیت های زیست محیطی چشمگیری که گفته شد، در کاهش هزینه های تولید نیز تأثیرگذار است.
در سال ۱۹۷۳ شرکت Alcoa اعلام کرد که پس از چندین سال تحقیقات موفق به ابداع روش جدیدی برای احیاء آلومینیوم شده و بر اساس آن کارخانه Palestine در تگزاس را با ظرفیت ۱۵۰۰۰ تن در سال و با توسعه احتمالی تا ۳۰۰۰۰ تن را بنا کرد. بخشی از این کارخانه در سال ۱۹۷۶ شروع بکار کرد. در این روش بجای اکسید آلومینیوم از کلرور آلومینیوم استفاده شده که پس از الکترولیز آن آلومینیوم آزاد میگردد. تولید کلرور آلومینیوم بوسیله راکتور که Al2O3 بسیار خالص و مخلوط شده با کربن را به AlCl3 تبدیل مینماید انجام میشود.
ادامه کار این روش با مشکلاتی همراه بوده که شرکت مذکور نتوانست آنها را حل نماید. از نکات جالب این روش، مصرف انرژی کمتر، حذف شدن فلوئور از محیط کار، درجه حرارت پائین الکترولیز و مصرف نشدن آندهای کربن است.
صنعت آلومینیوم از جمله صنایعی است که به سرمایهگذاری زیاد نیاز دارد و هر گزینه جدیدی که بتواند مقدار سرمایهگذاری به ازاء هر تن آلومینوم را کاهش دهد جالب و دنبالکردنی است.
بنظر میرسد که روش الکترولیز کلراید الومینیوم بتواند جانشین روش هال-هرولت بشود، زیرا اولاً دارای مصرف انرژی مناسبتری است و ثانیاً این احتمال وجود دارد که بتوان مستقیماً از بوکسیت یا خاک رس(Clay) آلومینیوم کلراید تهیه کرد که هزینه های تولید آلومینیوم را بشدت کاهش خواهد داد.
Aloca با ساخت واحد Palestine مورد اعتماد بودن این روش را اعلام کرده است. البته این واحد در حال حاضر مورد بهرهبرداری نمی باشد.
نتیجه اینکه در حال حاضر ، روش هال-هرولت پشتوانه اصلی صنعت تولید الومینیوم می باشد. بهرحال کاوش برای یافتن گزینه جدید ادامه خواهد داشت و شاید در سال های آینده روش قابل رقابت با روش هال-هرولت پیدا شود. در حال حاضر کارخانجات جدید نیز با روش هال-هرولت ساخته می شوند و تلاش ها در جهت افزایش هر چه بیشترآمپراژ و کاهش مصرف انرژی ادامه دارد و پروسه به سمت اتوماسیون و مکانیزه شدن بیشتر پیش میرود.
ویژگیهای قابل توجه
- سبکی وزن: در یک حجم مساوی، وزن آلومینیوم تقریباً یک سوم وزن فولاد ، مس و برنج است.یک متر مکعب آلومینیوم حدود ۷۷ کیلو گرم وزن دارد . در حالی که وزن یک متر مکعب فولاد ۲۲۰ کیلو گرم است.سبکی وزن در مصنوعات آلومینیومی از مزایای بسیار مهم تلقی می شود. سبکی وزن آلومینیوم علاوه بر کاهش هزینه های حمل و نقل آن، سبب شده است که از نظر قیمت با فولاد رقابت کند.
- نسبت بالای استحکام به وزن: تلفیقی از استحکام بالا و سبکی وزن، فقط در چند ماده در طبیعت وجود دارد. استحکام بالای برخی از آلیاژ های آلومینیوم قابل مقایسه با استحکام فولاد ها است. این مزیت سبب شده است تا آلومینیوم در صنایع خودروسازی، دفاعی و نظامی، هوا- فضا، ساختمانی ، حمل و نقل و بسته بندی کاربردد های گوناگونی را پیدا کند.
- قابلیت شکل پذیری : آلومینیوم را می توان با روش های مختلف شکل دادن فلزات، تغییر فرم داد. آلومینیوم به سادگی به صورت لوله، میله، صفحه، فویل و قطعات ریختگی با اشکال مختلف در می آید. مثلاً فویل های نازک ۰٫۰۰۴ میلی متر با روش نورد به راحتی امکان پذیر است.
آلومینیوم همچنین قابلیت اتصال به روش های جوشکاری ، لحیم کاری، چسب کاری و پرچ کاری دارد.
- خاصیت ارتجاعی: برخی از آلیاژ های آلومینیومی چنانچه در یک محدوده خاص تحت تاثیر نیرو یا ضربه قرار گیرند، پس از برداشتن نیرو می توانند دوباره حالت اولیه خود را به دست آورند. از این ویژگی آلومینیوم در طراحی و ساخت محصولاتی که به استحکام و انعطاف پذیری نیاز دارند. بسیار استفاده می شود.
- مقاومت در برابر خوردگی: سطح قطعات آلومینیوم زنگ نمی زند، زیرا آلومینیوم با اکسیژن هوا ترکیب می شود و یک لایه فشرده آلومینیوم تولید میکند. این لایه فشرده که ضخامت آن فقط چند هزارم سانتی متر است، مانع از تماس اکسیژن با لایه های زیرین آلومینیوم می شود و از اکسید شدن بیشتر قطعه جلوگیری می کند . بنابراین اکسید کردن سطوح قطعات آلومینیوم خوردگی آن در محیط های مختلف مانند هوای مرطوب، آب دریا و محدوده گسترده ای از سایر مواد فیزیکی و شیمیایی پیشگیری می نماید.
- هدایت حرارتی بالا : آلومینیوم بعد از نقره ، مس و طلا هادی ترین فلز است، به خاطر همین خاصیت در ساخت ظروف آشپزخانه، مبدل های حرارتی آبی و روغنی است.
- غیر سمی بودن: آلیاژهای جامد آلومینیوم که دارای لایه اکسیدی سطحی هستند غیر سمی اند و در صنایع بسته بندی مواد غذایی، دارویی و بهداشتی به طور گستردهای بکار می روند. بعلاوه آلومینیوم سطحی صاف و غیر متخلخل دارد که از جذب مواد خارجی و باکتری ها جلوگیری می کند.آلومینیوم می تواند در تماس بسیار نزدیک و فشرده با مواد غذایی قرار گیرد بدون اینکه بر روی طمع ، رنگ و بوی آن تاثیر بگذارد.
علاوه بر موارد استفاده فوق الذکر ، از آلومینیوم به اشکال مختلف در طبابت و جراحی استفاده می شود.برای خون بندی زخمها و تنگی نفس از پودر آلومینیوم استفاده می کنند.
- هدایت الکتریکی: در یک حجم مساوی، آلومینیوم مانند مس حدود ۶۲ درصد الکتریسته را از خود عبور می دهد.بعد از نقره مس و طلا بالاترین هدایت الکتریکی را دارا می باشد. اما در یک وزن برابر آلومینیوم می تواند دو برابر مس هادی الکتریسیته باشد. به این ترتیب استفاده از آلومینیوم در انتقال الکتریسته، بسیار مقرون به صرفه است. به همین دلیل در ایستگاه ها و نیروگاه برق ، عموماً از آلومینیوم استفاده می شود.
- قابلیت بازتاب نور: آلومینیوم قابلیت بازتاب بیش از ۸۰ درصد اشعه نور مریی و اشعه های نامریی که طول موج مریی در دو انتهای طیف نور را دارد. از این خاصیت در ساخت باز تابنده های نوری و ساخت صفحات محافظ در برابر نور ، امواج رادیویی و تشعشع های حرارتی مادون قرمز استفاده می شود. قابلیت های بازتاب نور در آلومینیوم سبب کاربرد این فلز در باطری های خورشیدی و گیرنده ها و فرستنده های الکترومغناطیس شده است. محصولات آلومینیومی باید بعد از ساخت پولیش شوند. تا حداکثر قابلیت بازتاب در آن ها بدست آید.
- وزن مخصوص کم: یک متر مکعب آلومینیوم خالص ۸/۲۸۲۷ کیلو گرم وزن دارد و یک متر مکعب از سنگین ترین آلیاژ های آلومینیوم دارای وزنی حدود ۲۹۵۳ کیلوگرم است. که این سنگین ترین آلیاژ های آلومینیوم حداقل ۱۶۷۸ کیلو گرم در هر متر مکعب سبکتر از وزن هم حجم سایر فلزات ساختمانی است. پس بنابراین این مزیت می تواند باعث : حمل نقل ارزانتر- ظرفیت بیشتر- صرفه جویی در کار – ممان اینرسی کمتر شود.
- غیر مغناطیسی بودن: از این ویژگی در ساخت آلیاژهای آلومینیومی برای کاربردهای الکتریکی و الکترونیکی از قبیل تجهیزات مجاور حوزه های پرقدرت مغناطیسی، سخت افزارهای فشار قوی، تجهیزاتی که در قطب نماهای مغناطیسی بکار می روند و وسایل حساس به مغناطیس استفاده فراوان می شود.
- عدم جرقه زایی: با اینکه آلومینیوم قابلیت هدایت الکتریکی بسیار بالایی دارد ، ولی جرقه تولید نمی کند. از این خاصیت بسیار مهم در وسایلی که در محیط های قابل اشتعال و انفجار به کار می روند استفاده می شود.
مشخصات شیمیایی آلومینیوم

آلومینیوم با عدد اتمی ۱۳ وجرم اتمی ۲۶٫۹۸ عنصری فلزی است که در گروه سوم (IIIA) جدول تناوبی (مندلیف) قراردارد. این بدان معناست که اتم آلومینیوم دارای ۱۳ الکترون در لایه اوربیتالی می باشد.
تعداد الکترونهای لایه آخر هر عنصر تعیین کننده ظرفیت آن عنصر است. آلومینیوم در لایه ظرفیت خود سه الکترون دارد وبه همین جهت عنصری سه ظرفیتی محسوب می گردد .
آلومینیوم فلزی نرم و سبک است که دارای ظاهر نقره ای کدر می باشد زیرا وقتی در معرض هوا قرار می گیرد، یک لایه نازک از اکسید آلومینیوم سریعا روی سطح آن تشکیل می شود. آلومینیوم با نماد Alوزن مخصوص ۲٫۷۵ گرم بر سانتی متر مکعب، نقطه ذوب ۶۶۰٫۲۵ درجه سانتی گراد و نقطه جوش آن ۲۷۵۰ درجه می باشد. آلومینیوم در اسیدها کم محلول است ولی در بازهای قوی بخوبی حل می شود . بنابر این، آلومینیوم برای ذخیره اسید نیتریک، اسید سولفوریک غلیظ، اسیدهای آلی و دیگر واکنش گرها و مواد شیمیایی مورد استفاده قرار می گیرد. با این وجود، پوشش اکسیدی آن در محلول های قلیایی حل می شود و خوردگی آن ها سریع است که منجر به تولید هیدروژن و آلومینات فلزات قلیایی می شود.
آلیاژهای آلومینیوم
آلیاژهای آلومینیوم به دو گروه بزرگ آلیاژهای ریختگی (Alloys Casting) و کارپذیر یا نوردی (Alloys wrought) تقسیم می شوند، که آلیاژ های نوردی بیش از ۸۰ درصد حجم کل آلیاژهای مصرفی آلومینیوم را در بر می گیرند.
آلیاژهای کار پذیر یا نوردی : آلیاژهای نوردی بر اساس استاندارد(A.A (Associatian Aluminium به هشت گروه ۱xxx تا ۸xxx بر اساس نوع فلزات تشکیل دهنده تقسیم می شوند؛ آلیاژهای کارپذیر آلومینیومآلیاژ هایی هستند که از طریق مکانیکی به شکل مورد نظر در می آیند. برخی از این آلیاژ ها را می توان توسط عملیات حرارتی خاص تقویت نمود و برخی دیگر قابل عملیات حرارتی نیستند. آلیاژ های کار پذیر بر اساس عنصر اصلی آلیاژی خود به هشت گروه تقسیم و هر یک از آلیاژهای هر گروه توسط A.A (جامعه آلومینیوم ) ، با یک عدد چهار رقمی نام گذاری گردیده اند.
آلیاژهای ریختگی : آلومینیوم آلیاژهایی هستند که از طریق ریخته گری به شکل مورد نظر در آورده می شوند. این آلیاژها نیز برخی قابل عملیات حرارتی و بعضی غیر قابل عملیات حرارتی هستند. هریک از این آلیاژها نیز توسط A.A با یک عدد چهار رقمی که بین ارقام چهارم و سوم از سمت چپ یک نقطه قرار گرفته است نام گذاری گردیده اند.
کاربردها
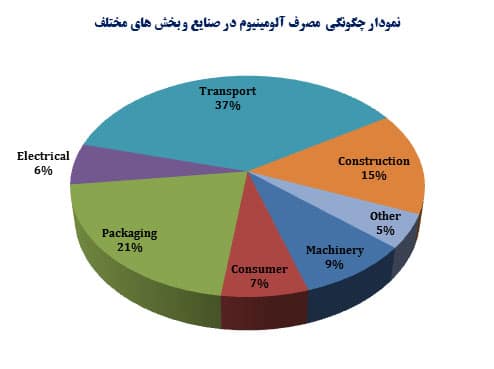
ترکیب منحصر به فرد و خواص عالی آلومینیم باعث شده است این فلز یکی از مهمترین مواد مهندسی و ساخت مصالح به شمار آید. جرم سبک ،استحکام به وزن بالا و مقاومت بالا در مقابل خوردگی و زنگ زدگی آلومینیم را تبدیل به یک فلز عالی نموده است. آلومینیم قابل بازیافت است و با محیط زیست سازگار است. آلومینیم با دوام است و سالها بدون پوسیدگی کار می کند. چه از نظر کیفیت و چه از نظر ارزش آلومینیم کاربردی ترین فلز بعد از آهن به شمار می آید و تقریبا در تمامی بخش های صنعت دارای اهمیت می باشد.
همه این ویژگی های آلومینیوم را به یک گزینه مناسب جهت کاربرد در شرایط خاص تبدیل نموده است. موارد استفاده آلومینیوم در حمل ونقل، بسته بندی، ساخت و ساز، برق و… می باشد.
چه از نظر کیفیت و چه از نظر ارزش، آلومینیوم کاربردیترین فلز بعد از آهن است و تقریبأ در تمامی بخشهای صنعت دارای اهمیت میباشد. آلومینیوم خالص، نرم و ضعیف است، اما میتواند آلیاژهایی را با مقادیر کمی از مس، منیزیوم، منگنز،سیلیکون و دیگر عناصر بوجود آورد که این آلیاژها ویژگیهای مفید گوناگونی دارند. این آلیاژها اجزای مهم هواپیماها و راکتها را میسازند.
وقتی آلومینیوم را در خلاء تبخیر کنند، پوششی تشکیل میدهد که هم نور مرئی و هم گرمای تابشی را منعکس میکند. این پوششها لایه نازک اکسید آلومینیوم محافظ را بوجود میآورند که همانند پوششهای نقره خاصیت خود را از دست نمیدهند. یکی دیگر از موارد استفاده از این فلز در لایه آینههای تلسکوپهای نجومی است.
- متالوژی:
آلومینیوم به همراه درصد کمی سیلیس، روی منگنز، منیزیم، مس و یا لیتیوم، آلیاژهای مقاومی در برابر فرسودگی، و زنگ زدن را تشکیل می دهد که برای بسته بندی، ظروف، کالاهای الکتریکی، مصالح ساختمانی، هوا فضا و اتومبیل سازی به کار می رود.
- شیمیایی:
آلومینیوم برای تهیه انواع عایق و به عنوان یک رسانای خوب گرمایی، در تهیه وسایل آشپزخانه به کار می رود. آلومینیوم بعد از مس، دومین عنصر رسانای جریان الکتریکی است و به علت ایجاد خطوط بسیار قوی الکتریکی، از آن برای تهیه سیم های انتقال ولتاژ بالای جریان استفاده می شود. بوکسیت ها در تهیه سیمان و ماده ثابت رنگ کاری به کار می روند و همچنین از پودر اکسید آلومینیوم به صورت کانی بوکسیت، برای تهیه سولفات آلومینیوم و آلومینات سدیم در تصفیه آب استفاده می شود. از سولفات آلومین نیز در صنایع کاغذسازی و پارچه بافی استفاده می شود.
- بازیافت
آلومینیوم به طور کامل قابل بازیافت(۹۰%) است و ۹۵ درصد نیز قابلیت ذخیره انرژی دارد. قراضه آلومینیوم در بازار جهانی مورد معامله قرار می گیرد. قراضه های آلومینیوم به طورگسترده به ذوب کنندگان آلومینیوم ثانویه فروخته می شود. این روش هم به حفظ و سلامت محیط زیست کمک می کند و هم از نظر تجاری مقرون به صرفه است؛ چراکه در هزینه ذوب و تولید آلومینیوم از نظر مصرف انرژی صرفه جویی می شود.
- صنعت حمل و نقل
الف- اتومبیل ها
مزایای کاربرد آلومینیم در خودرو
امروزه با وجود رقابتهای جهانی و افزایش ارتباط محیطی ، تولید کنندگان ماشین با رقابتهای جدیدی مواجه شده اند ، تولیدات آنها باید آلودگی کمتری ایجاد کند . و به سادگی مجدداً وارد چرخه ماشین ها بشود ، بدون اینکه امنیت و راحتی آن کاهش یابد ، کارآیی ماشین (تولید) بالا رود و هزینه جاری کاهش یابد . هر ۱۰۰ کیلو گرم کاهش وزن، سبب می شود که ۰٫۶ لیتر در ۱۰۰ کیلو متر، سوخت مصرفی کاهش یابد . گاز کمتری از اگزوز ماشین خارج شود و هزینه کاهش می یابد . آلومینیم یک عامل اساسی برای کاهش وزن است .این کاهش وزن باعث افزایش بهره وری و مصرف کمتر سوخت در خودرو شده است.
کاربرد زیاد آلومینیوم در وسایل نقلیه، میتواند تا حدود ۲۰درصد انتشار گازهای گلخانهای جهان را کاهش دهد. مصرف زیاد آلومینیم در خودرو باعث شده است که از ۱۹۹۰ تاکنون بیش از ۳۵ بیلیون گالن سوخت صرفهجویی شود.
ب- صنایع هوافضا
آلیاژهای آلومینیوم به سبب مقاومت بالا در برابر کشش به نسبت وزن کم آن، استفاده زیادی در ساخت هواپیماهای تجاری و نظامی دارند. آلومینیوم ماده برتر استفاده شده در هواپیماست که از ۵۵ تا ۸۱ درصد کل وزن آن را تشکیل می دهد.
نسل جدید آلیاژهای آلومینیوم- لیتیومی، وزن هواپیما را ۲۵ درصد کاهش میدهد. این آلیاژها دارای چگالی کمتر، چقرمگی بالا و مقاومت دربرابر تخریب بیشتری نسبت به مواد بهکار رفته قبلی در صنعت هوا-فضاست. نخستین نسل آلیاژهای آلومینیوم-لیتیومی در صنایع هوا-فضا و صنایع دفاع بهکار رفتهاند. این آلیاژها اولینبار در ایرباس ۳۸۰A مورد استفاده قرار گرفتند. پس از آن بوئینگ۷۸۷ مورد تحول قرار گرفت و از این آلیاژ در تولید محصولات خود بهره برد .استفاده از آلیاژهای آلومینیوم-لیتیومی در هواپیماسازی نسبت به مصرف کامپوزیتها، مصرف سوخت را ۲۷-۲۲ درصد و وزن هواپیما را ۱۰-۶ درصد کاهش میدهد. درعینحال مقاومت به خوردگی و ساختار بدنه هواپیما ۱۰۰ درصد بهبود مییابد. بهنظر میرسد با ورود نسل جدید آلیاژهای آلومینیوم-لیتیومی به بازار آینده مثبتی در انتظار صنایع هواپیماسازی باشد.
ج- صنایع دریایی
آلومینیوم موارد استفاده های زیاد و متنوعی در صنایع کشتی سازی دارد. علت استفاده آلومینیوم در این صنایع وزن سبک، مقاومت بالا و ایستادگی آن در برابر خوردگی است. آلیاژهای آلومینیم گروه ۶۰۰۰ استحکام و مقاومت به خوردگی خوبی در سازههای دریایی دارند. بازار استفاده از آلومینیوم به خصوص در قایق های تندرو بیشتر است. مهمترین و بزرگترین پتانسیل استفاده از آلومینیوم در این صنعت، کشتی های مخصوص حمل مسافر و بار است که می خواهند از سرعت زیادی نیز برخوردار باشند.
د- صنایع حمل و نقل ریلی
مقاومت بالا به نسبت وزن کم آلومینیوم سبب می شود که از آن در ساخت قسمت های چرخشی قطارها استفاده شود که به قطار اجازه می دهد تا سوخت و بار بیشتری را حمل نماید. آلومینیوم اغلب در برابر زنگ زدن مقاوم است که باعث می شود بتوان از آن در مصارف طولانی مدت استفاده نمود. آلومینیوم در این صنعت، مصارف متنوع و گوناگونی دارد که می توان به ساخت واگن های حمل بار و مسافر، لکوموتیوها و مترو اشاره کرد. ریل هایی از جنس آلومینیوم می توانند در انواع سیستم ریل مغناطیسی گسترش یابند. در ترن های سریع السیر نیز که برای حمل مسافر از آنها استفاده می شود از آلومینیوم استفاده می شود.
- قوطی ها وبسته بندیها
استفاده از آلومینیوم در بدنه و سر و ته قوطی های کنسرو، مهمترین استعمال آلومینیوم در این بخش از صنعت است که۹۰درصد آن را تشکیل می دهد. صنایع بسته بندی، دومین صنعت بزرگ استفاده از آلومینیوم بعد از صنعت حمل و نقل هستند، ولی مقادیر بسیار متفاوتی از آلومینیوم در این صنعت در کشورهای جهان مصرف می شود.
- صنعت ساختمان
صنعت ساختمان، بازار مهمی برای آلومینیوم است که در آن آلومینیوم و آلیاژهای آن مورد استفاده قرار می گیرند. مهمترین فاکتورهایی که باعث می شوند از آلومینیوم در این قسمت استفاده شود، وزن کم، شکل پذیری بالا، مقاومت بالا در برابر زنگ زدگی، هزینه کم برای نگهداری، عمرطولانی و عدم نیاز به رنگ کردن است. وزن کم آلومینیوم باعث می شود که هزینه احداث بنا پایین آمده، زمان ساخت نیز کاهش یابد. چین و آمریکا بزرگترین مصرف کننده گان آلومینیوم در ساختمان سازی هستند.
- صنایع برق
منیزیم و سیلیس برای افزایش خواص فیزیکی آلومینیوم به آن اضافه می شوند تا آلیاژی مقاوم از آلومینیوم بسازند. اما آلیاژ حاصل، خاصیت هدایت الکتریکی ضعیف تری نسبت به آلومینیوم خواهد داشت. آلومینیوم ۶۰ درصد هدایت الکتریکی مس را دارد، ولی چگالی آن بسیار کمتر از مس است (۶/۲ در برابر۹ ) وزن رساناهای ساخته شده از آلومینیوم کمتر از نصف وزن رساناهای مسی است.
از دهه ۱۹۲۰ تاکنون آلومینیوم برای قسمت بالای دکل های انتقال برق فشار قوی به کار می رود. استحکام بالا به نسبت وزن کم، باعث می شود که بتوان با آن دکل های بلند و مستحکمی ساخت که باعث کاهش قیمت در سیستم انتقال نیرو می شود. آلومینیوم اغلب در برابر خوردگی مقاوم است.
- مصارف وسایل با دوام
کولرها، یخچال ها و فریزرها و ماشین لباسشویی، بخش عمدهای از کل تقاضای آلومینیوم را تشکیل می دهند. استفاده از آلومینیوم در این سه صنعت در ۱۵ سال اخیر ۲ برابر شده است. البته استفاده از آلومینیوم در وسایل پخت وپز مثل اجاق گاز، رو به کاهش نهاده است، زیرا گفته شده که می تواند باعث بیماری آلزایمر شود. این فلز از آن جهت در این صنعت مورد استفاده قرار می گیرد که قابلیت انتقال گرمای بالایی دارد، وزن سبکی دارد و در مقابل خوردگی مقاوم است.
- ماشین ها و تجهیزات
این بخش شامل صنایع کشاورزی، ساختمان سازی و تجهیزات کارخانه هاست. این موارد شامل لوله های آبیاری، نردبان ها، داربست ها، وسایل اتصاالت و سخت افزارهای دیگر است
- تصفیه وگالوانیزه کردن فولاد
آلومینیوم در پروسه های مدرن تولید فولاد و برای پالایش فولاد به کار می رود. آلومینیوم به فولاد اضافه می شود تا خصوصیات مکانیکی (فیزیکی) فولاد را بهبود بخشد. آلومینیوم به فولادهای دارای کربن کم اضافه می شود تا با کاهش میزان نیتروژن، میزان کشش آن را افزایش دهد. یکی از مصارف مهم آلومینیوم، استفاده از آن به عنوان محافظ ورقه های فولاد برای جلوگیری از زنگ زدگی است. این ترکیب پوشاننده فولاد، شامل ۵۵% آلومینیوم، ۵/۴۳ %روی و ۵/۱ %سیلیسیم است. استفاده اصلی از آهن گالوانیزه و ترکیبات مشابه آن در صنایع اتومبیل سازی است که معمولاً برای خطوط انتقال سوخت، خطوط خنک کننده روغن و خطوط هدایت نیرو به کار می رود.
- باتری ها
آلومینیوم در موارد متعددی برای تولید و ذخیره سازی انرژی الکتریکی مورد آزمایش قرار گرفته است. استفاده از باتری های آلومینیوم هوا بخصوص در ماشین هایی که با انرژی الکتریسیته فعالیت می کنند، گسترش یافته است. البته این میزان در ماشین های دیگری که انرژی کمتری مصرف می کنند نیز گسترش یافته است. از سال ۱۹۸۸ تلاشی آغاز شده تا باتری های آلومینیوم هوا در مراکز سوییچ مخابراتی، جایگزین باتری های سرب اسید شوند. باتری های این مراکز باید دارای شرایط ویژه ای باشند که سعی شده در محصولات تولید لحاظ شود. این باتری ها بعنوان ذخیره باتری های سرب- اسید فعالیت می کنند و یا باتریی های که در صورت نقص در باتریهای سرب- اسید از آنها جهت امور مخابراتی استفاده میشود.
- نیمه رساناها
آلومینیوم یکی از موادی است که پتانسیل لازم برای تولید رساناهای با قدرت بالا را داراست. رساناهای با قدرت بالا، مواد یا آلیاژهایی هستند که مقاومتی در برابر جریان برق ندارند وآن را بدون اتلاف انرژی و به سرعت منتقل می نمایند. بیشتر رساناهای با قدرت بالای که تاکنون گسترش یافته اند، فقط در دمای بسیار پایین، فعالیت می کنند.
- سایر مصارف
استفاده دیگر آلومینیوم در مهمات سازی است که البته اندک است. از آلومینیوم در تفنگ ها استفاده می شود تا قابلیت و کارایی آنها بالا رود. در بعضی موارد هم در کلت های کمری نیروهای پلیس و در بعضی از کشورها در ضرب سکه به کار می رود. از پودر آلومینیوم در صنایع معدنی نیز استفاده می شود.
منابع و استخراج آلومینیوم
آلومینیوم خالص در طبیعت بسیار کمیاب و بندرت یافت میشود. ترکیبات آلومینیوم موجود در طبیعت در منابع مختلفی نظیر سنگهای آذرین، سنگهای رسوبی و مانند آن یافت میشود. مهمترین کانی تجاری آلومینیوم بوکسیت(Bauxite) است . در سال ۱۸۲۱ میلادی در شهر لس بوکس کشور فرانسه کشف شد.
بوکسیت مخلوطی از هیدروکسید آلومینیوم، اکسید یا هیدروکسید آهن، اکسید تیتانیوم، سیلیکاتهای آلومینیوم، کائولین و مقدار کمی از مواد دیگر میباشد .
میزان کلی ذخائر جهانی بوکسیت ۳۳ میلیارد تن برآورد شده که حدود ۷۵ درصد آن در ۵ کشور گینه، استرالیا، برزیل، جامائیکا و هند است. در ایران نیز در مناطق آباده ، جاجرم و … ذخایر بوکسیت وجود دارد.

در حال حاضر بیش از ۹۸% آلومینای جهان از بوکسیت تولید میشود . نسبت میزان AL2O3 به SiO2 که مدول نامیده میشود یکی از مبانی ارزیابی کیفیت بوکسیت است . بوکسیت مرغوب به بوکسیتی گفته می شود که مدول آن بیش از ۱۰ باشد.
یکی دیگر از معیارهای رتبهبندی بوکسیت علاوه بر مدول، حداقل مقدار آلومینا در آن است . در روش بایر که روش اصلی تولید تجاری آلومینا از بوکسیت است، حداقل رقمی که برای آلومینای موجود در بوکسیت در نظر گرفته شده بر حسب نوع بوکسیت بین ۳۰ تا ۴۵ درصد میباشد.
تقریبا به ازای هر تن ۲ تولید آلومینا به طور متوسط نیاز به ۴ تن بوکسیت بسیار مرغوب است و با کاهش درجه مرغوبیت و عیار (درصد آلومینا یا Al2O3 در بوکسیت) و کاهش نسبت مدول (نسبت عیار آلومینای موجود به عیار سیلیس در بوکسیت)، مصرف بوکسیت افزایش یافته و حتی تا ۶ تن هم می رسد .
آلومینیوم یک فلز واکنشگر است و نمیتواند از سنگ معدن خود بوکسیت (Al۲O۳) بهوسیله کاهش با کربن جدا شود. در عوض روش جداسازی این فلز از طریق برقکافت است. (این فلز در محلول اکسیده شده، سپس بصورت فلز خالص جدا میشود) لذا جهت این کار، سنگ معدن باید درون یک مایع قرار بگیرد. اما بوکسیت دارای نقطه ذوب بالایی است (۲۰۰۰۰ درجه سانتیگراد) که تأمین این مقدار انرژی از نظر اقتصادی مقرون به صرفه نیست.
برای سالهای زیادی بوکسیت را در فلورید سدیم و آلومینیوم مذاب قرار میدادند و نقطه ذوب آن تا ۹۰۰درجه سانتیگراد کاهش مییافت. اما امروزه مخلوط مصنوعی ازآلومینیوم، سدیم و فلوئورید کلسیم، جایگزین فلورید سدیم و آلومینیوم شدهاست. این فرایند هنوز مستلزم انرژی بسیار زیاد است و کارخانجات آلومینیوم دارای ایستگاههای برق مخصوص خود در اطراف این کارخانهها هستند.
الکترودهایی که در الکترولیز بوکسیت بکار میروند، هر دو کربن هستند. وقتی سنگ معدن در حالت مذاب است، یونهای آن آزادانه حرکت میکنند. واکنش در کاتد منفی اینگونهاست:

در اینجا یون آلومینیوم در حالت کاهش است (الکترونها اضافه میشوند). سپس فلز آلومینیوم به سمت پایین فرومیرود و خارج میشود.
آند مثبت، اکسیژن بوکسیت را اکسیده میکند که بعد از آن با الکترود کربنی واکنش کرده تا تولید دیاکسید کربن نماید.
این کاتد باید عوض شود، چون اغلب تبدیل به دیاکسید کربن میشود. بر خلاف هزینه الکترولیز، آلومینیوم فلزی، ارزان با کاربرد وسیع است. امروزه آلومینیوم را میتوان از خاکه معدنی استخراج کرد، اما این فرایند، اقتصادی نیست.
فرآیند تولید آلومینیوم – فرآیند احیاء
در این فرآیند جهت تولید شمش آلومینیوم از الکترولیز نمک مذاب استفاده می نمایند مواد اولیه اصلی در این طرح شامل آلومینا و فلورایدها می باشند. جریان برق DC جهت الکترولیز مورد نیاز است که توسط رکتیفایرها تأمین میگردد. تحت تأثیر این جریان مستقیم برق DC اکسید آلومینیوم (آلومینا) به آلومینیوم خالص تبدیل میشود. جهت تولید آلومینیوم از دیگهایی بنام دیگ الکترولیز که شامل آند و کاتد می باشد و بطور مخصوصی بر روی استراکچرهای فولادی قرار میگیرند استفاده می شود.
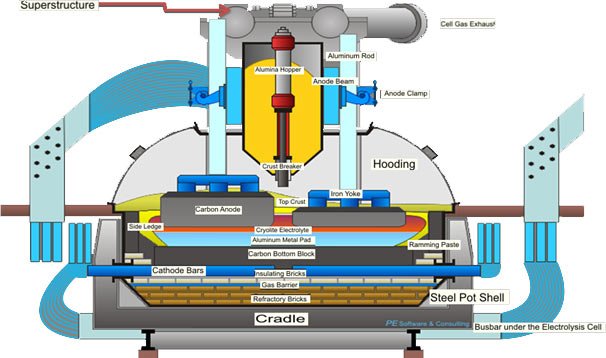
در این فرآیند کریولیت ، آلومینیوم فلوراید ، کلسیم فلوراید و آلومینا بعنوان الکترولیت و مواد کربنی بعنوان الکترود عمل مینمایند. آلومینیوم مذاب در کاتد رسوب و گاز آندی که غالباً Co2 میباشد در آند تولید میگردد. در طی فرآیند گازهای هیدروژن فلوراید و غبار تولید میگردد که همراه گاز آندی مجموعاً بخارات احیا را تشکیل میدهد. در دماهای کمتر از محدوده ۶۰۰-۴۰۰ درجه سانتیگراد ممکن است آلومینـا حاوی ۵/۰-۲/۰ درصد رطوبت باشد که این رطوبت با فلورایدهای جامد در درجه حرارتهای بالا واکنش میدهد.
۲Na3AlF6+3H2O >>>>>>>>> Al2O3+6NaF+6HF
۲AlF3+3H2O >>>>>>>>> Al2O3+6HF
بخارات احیاء در سالن احیاء منتشر شده و شرایط کار را نامطلوب و اثرات جدی روی سلامتی کارگران دارد بعلاوه این بخارات اثرات سوء زیست محیطی را به همراه دارد بنابراین از ضروریترین امور در این فرآیند جمعآوری هر چه بیشتر این بخارات میباشد تا علاوه بر حذف این گازها و بخارات مضر ، آلومینا و فلورایدها بازیابی گردند. در این فرآیند اکسید آلومینیوم مورد نیاز پس از انتقال به کارگاه احیاء به همراه فلورایدها به داخل مخازن ثابت ریخته میشوند. در سیستم کنترل آلودگی جهت جذب گازهای دیگ باید از آلومینای تازه استفاده گردد که این نیز به نوبه خود بعنوان آلومینای غنی شده بداخل اوربینهای دیگ انتقال داده می شود و آلومینای داخل اوربین بصورت خودکار و اتوماتیک و مداوم بداخل حوضچه مذاب انتقال مییابد.
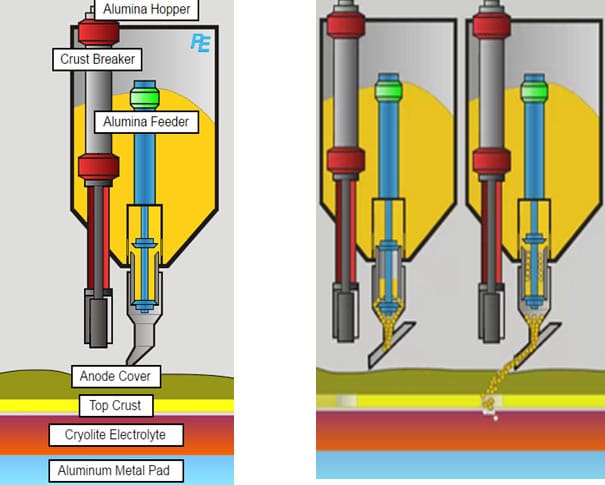
بلوکهای کربن آندی در کارگاه میله گذاری تکمیل شده و در کارگاه احیاء با آندهای کارکرده معاوضه و این آندها بار دیگر به کارگاه میله گذاری انتقال مییابد.
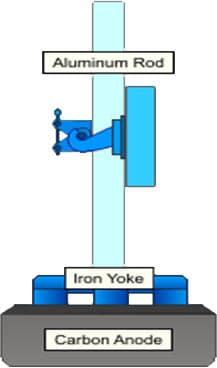
جریان برق DC حاصل از رکتیفایرها توسط خطوط انتقال باسبار جهت الکترولیز وارد کارگاه احیاء میشود ، آلومینیوم مذاب موجود در دیگ از طریق سیستم مکش تخلیه شده و به کارگاه ریخته گری انتقال مییابد و در آنجا وارد کورههای نگهدارنده شده و با افزایش عمل اختلاط بر حسب نیاز محصولات متنوعی از آن تولید میگردد.
همواره مقداری از آلومینیوم مذاب کارگاه احیاء داخل پیگ ریخته میشود تا جهت ذوب مجدد بکار گرفته شود و قبل از انجام فرآیند و در حین آن آزمایشهایی شامل کنترل و آنالیز مواد خام مصرفی و تولیدی صورت می گیرد تا محصول بدست آمده بر اساس استانداردهای قابل قبول تولید گردد. در خاتمه فرآیند شمش های آلومینیوم تولید شده مورد ارزیابی و کنترل نهایی قرارگرفته پس از بستهبندی و توزین جهت توزیع به انبار فرستاده میشود.
آلیاژهای آلومینیوم
آلیاژهای آلومینیوم آلیاژهایی با خاصیت فلزی هستند که معمولاً شامل ۹۰–۹۶٪ آلومینیوم بوده و علاوه بر آن دارای یک یا چند عنصر دیگر هستند که به منظور بهبود خواص به آلومینیوم افزوده شدهاند. معمولاً این آلیاژهای علاوه بر عناصر آلیاژی اصلی شامل چندین عنصر آلیاژی فرعی نیز هستند که مقدار بسیار کمی داشته ولی تأثیر زیادی بر خصوصیتهای آنها دارند.
عناصر آلیاژی
اگرچه بسیاری از فلزات با آلومینیوم تشکیل آلیاژ میدهند ولی تعداد کمی از آنها در آلومینیوم حلالیت قابل توجهی دارند که به عنوان افزودنی آلیاژی اصلی بکارروند. در بین عناصر آلیاژی معمول تنها روی، منیزیوم، مس و سیلسیوم حلالیت بالایی دارند.
آلیاژهای کارشده:
- مقاومت به خوردگی: بسیاری از آلیاژهای آلومینیوم به علت تشکیل طبیعی لایهٔ اکسیدی چسبنده به سطح مقاومت به خوردگی اتمسفری و شیمیایی بالایی دارند. این مشخصه در آلیاژهای سری ۱xxx، ۳xxx، ۵xxx و ۶xxx بارزتر است.
- رسانایی حرارتی: آلومینیوم و آلیاژهای آن رسانایی حرارتی بالایی دارند و با اینکه نسبت به فولاد در دمای پایینتری ذوب میشوند، اما در صورت مجاورت با آتش دمای آنها کندتر افزایش مییابد.
- رسانایی الکتریکی: آلومینیوم و برخی از آلیاژهای آن رسانایی الکتریکی بسیار بالایی داشته و از این لحاظ در میان فلزات رسانای تجاری پس از مس در ردهٔ دوم قرار میگیرند.
- نسبت استحکام/وزن: آلومینیوم با چگالی کم خود برای ساخت آلیاژهای مهندسی مناسب است. گر چه استحکام آلیاژهای پایه آلومینیوم به اندازه استحکام قابل حصول در فولادها نیست ولی نسبت استحکام به وزن این آلیاژها بالا بوده و به این دلیل آلیاژهای تجاری آلومینیوم تعداد زیادی دارند. استحکام اغلب این آلیاژ را میتوان از طریق رسوبسختی یا کار گرم افزایش داد.[۴]
- چقرمگی شکست: بسیاری از آلیاژهای آلومینیوم چقرم بوده و در کاربردهایی که مقاومت به شکست ترد و رشد ترک موردنیاز باشد بکار گرفته میشوند.
- کارپذیری: آلومینیوم و آلیاژهای آن را میتوان در بسیاری از روشهای فلزکاری که نیاز به کارپذیری دارند (مانند اکستروژن) بکار گرفت
- سهولت اتصال: آلومینیوم و آلیاژهای آن را میتوان با طیف گستردهای از روشهای تجاری معمول از قبیل جوشکاری، لحیمکاری، پیچکاری، پرچکاری و حتی میخزنی به یکدیگر اتصال داد.
- قابلیت بازیافت: بازیافت آلومینیوم و آلیاژهای آن در میان مواد سازهای بسیار ساده است و میتوان پس از بازیافت آنها را مستقیماً به صورت محصولات کیفیت بالا بکار برد.
آلیاژهای ریختهگی:
بطور کلی خواص آلیاژهای کارشده در آلیاژهای ریختهگی نیز وجود دارد ولی در انتخاب آلیاژهای ریختهگی خواص زیر اهمیت دارند:
- سهولت ریختهگری: این خصوصیت در سری سیلسیم بالای ۳xx.x بارز است. میزان بالای سیلسیم باعث جریانپذیری خوب و پرشدن قالب میشود.
- استحکام: آلیاژهای سری ۲xx.x استحکام بسیار بالایی دارند ولی ریختهگری آنها سختتر بوده و قابلیت پرداخت خوبی ندارند.
- پرداخت کار: سری ۵xx.x و ۷xx.x به علت قابلیت پرداخت خوب مورد توجهاند اما ریختهگری آنها از گروه ۳xx.x سختتر است.
نامگذاری
آلیاژهای آلومینیوم ریختگی و کارشده توسط شمارههای معینی مشخص میگردند. این شمارهها نشان میدهند که در فرایند ساخت چه عناصری به آلیاژهای فوق اضافهشده و گروه ویژهای از این فلزات را ساختهاند.
ANSI و AA
در سیستم نامگذاری ANSI و (AA (Aluminum Association برای آلیاژهای کارشده از یک مکانیزم شمارهدهی چهاررقمی و برای آلیاژهای ریختگی از سیستم شمارهدهی سهرقمی استفاده میشود که اولین عدد، معرف گروهبندی فلز و مهمترین عنصر آلیاژی اضافهشده به آلیاژ است.
| سری | ترکیب |
|---|---|
| ۱XXX | آلومینیوم تقریباً خالص |
| ۲XXX | آلیاژ آلومینیوم و مس |
| ۳XXX | آلومینیوم منگنزدار |
| ۴XXX | آلومینیوم سیلیسیمدار |
| ۵XXX | آلیاژ آلومینیم و منیزیم |
| ۶XXX | آلیاژهایی با ترکیب منیزیم، سیلیسیم و آلومینیوم |
| ۷XXX | آلیاژهایی با ترکیب روی و آلومینیوم و منیزیم |
| ۸XXX | آلیاژ آلومینیوم با عناصر کمتر متعارف همچون لیتیم |
| سری | ترکیب |
|---|---|
| ۱xx.x | آلومینیوم تقریباً خالص |
| ۲xx.x | آلیاژ آلومینیوم و مس |
| ۳xx.x | آلومینیوم داری مس، سیلسیم و اندکی منیزیم |
| ۴xx.x | آلومینیوم سیلیسیمدار |
| ۵xx.x | آلیاژ آلومینیم و منیزیم |
| ۶xx.x | آلیاژهایی با ترکیب منیزیم، سیلیسیم و آلومینیوم |
| ۷xx.x | آلیاژهایی با ترکیب روی و آلومینیوم و منیزیم |
| ۸xx.x | آلیاژ آلومینیوم با عناصر کمتر متعارف همچون قلع و لیتیم |
پسوندها نام گذاری
علاوه بر شماره گذاری آلیاژها، برای مشخص کردن یک آلیاژ نوع فرایند عملیات حرارتی یا فرایند ساخت آلیاژنیز مبنای شماره گذاری است. برای این نامگذاری از حروف انگلیسی در انتهای نام آلیاژ استفاده میشود، مثلاً AA 2024-T4. این نام گذاری تحت استاندارد ملی آمریکا با شماره ANSI H35.1 و با عنوان سیستم تعریف شده تمپر نامیده میشود و برای تمامی روشهای تولید کاربرد دارد. بسته به نوع فرایند تولید یکی از حروف F برای بدون تغییر و حالت از تولید، O برای آنیل، H برای سخت کردن کرنشی، W برای عملیات حرارتی محلول سازی و T برای عملیات حرارتی دیگر از جمله رسوب سختی برای نامیدن آلیاژها بکار میرود.
بصورت کامل تر:.
- Fبرای حالت بدون تغییر و از تولید
- Oبرای حالت آنیل شده
- Hبرای حالت کرنش سخت شده (کار سرد شده):
برای عدد اول در رده HXX
H1کرنش سخت شده بدون عملیات حرارتی
H2کرنش سخت شده و جزیی آنیل شده
H3کرنش سخت شده و پایداره شده از طریق عملیات حرارتی دمای پایین
عدد دوم در رده HXX (در صورت وجود) بیانگر مقدار سختی به دست آمده نسبت به حالت سختی حداکثر در آن عملیات سخت کاری است.
HX2بیانگر سختی به میزان ۱/۴ سختی حداکثر است.
HX4بیانگر سختی به میزان ۱/۲ سختی حداکثر است.
HX6بیانگر سختی به میزان ۳/۴ سختی حداکثر است.
HX8بیانگر سختی به میزان حداکثر است.
HX9بیانگر سختی بیشتر از سختی حداکثر است.
Tبرای حالتی است که آلیاژها تحت عملیات حرارتی قرار گرفته باشند. این حالت بیانگر تمپرهایی است که پایدار هستند (البته به غیر از حالات Fو O یا H)، بر خلاف حالت نام گذاری W.
T1سرد شده از یک فرایتد شکل دهی، با درجه حرارت بالا و پیر شده به صورت طبیعی
T2سرد شده از یک فرایتد شکل دهی، با درجه حرارت بالا، کار سرد شده و پیر شده به صورت طبیعی
T3عملیات حرارتی از نوع محلول سازی شده، کار سرد شده و پیر شده به صورت طبیعی
T4عملیات حرارتی از نوع محلول سازی شده و پیر شده به صورت طبیعی
T5سرد شده از یک فرایتد شکل دهی با دمای بالا و پیر شده به صورت مصنوعی
T6عملیات حرارتی از نوع محلول سازی شده و پیر شده به صورت مصنوعی
T7عملیات حرارتی از نوع محلول سازی شده و پایدار شده
T8عملیات حرارتی از نوع محلول سازی شده، کار سرد و پیر شده به صورت مصنوعی
T9عملیات حرارتی از نوع محلول سازی شده، پیر شده به صورت مصنوعی و سپس کار سرد شده
T10سرد شده از یک فرایتد شکل دهی با درجه حرارت بالا، کار سرد شده و پیر شده به صورت مصنوعی
در بعضی موارد پسوندهای رده T دارای اعدادی بیش از یک رقم هستند مانند AA 224-T351 یا AA 6061-T651 که در این صورت باید موارد زیر را در نظر داشت
TX51بیانگر تنش زدایی بوسیله کشش بعد از عملیات حرارتی عدد اول (عدد x)است.
TX52بیانگر تنش زدایی بوسیله تنش فشاری بعد از عملیات حرارتی عدد اول (عدد x)است.
TX54بیانگر تنش زدایی بوسیله ترکیبیاز کشش و فشاربعد از عملیات حرارتی عدد اول (عدد x)است.
TX6بیانگر کار سرد به وسیله نورد تا کاهش ۶ درصد از سطح مقطع، بعد از محلول سازی و سرد کردن است.
UNS
در سیستم نامگذاری UNS یا سیستم یکپارچه نام گذاری، آلیاژها با یک عدد پنج رقمی مشخص میگردد. برای تمامی آلیاژهای آلومینیوم اولین رقم ۹ است و چهار رقم بعدی مانند سیستم نام گذاری AA است. مثلاً UNS 92XXX به آلیاژی از آلومینیوم و مس اشاره دارد.



 English
English





